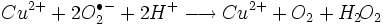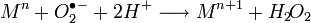sod =
superoxide dismutase = unieke anti-oxidant

Onderzoek bij cavia's voor uw cavia.
29 april 1993, NRC
Handelsblad, 1200 woorden:
Als radicalen al te vrij worden,
superoxide-dismutase beschermt tegen ALS
Amyotrofische
lateraalsclerose (ALS) kan veroorzaakt worden door
een mutatie in een enzym dat zorgt voor het
onschadelijk maken van vrije radicalen. ALS is een
ziekte, waarbij de zenuwcellen te gronde gaan in de
hersenschors en in het ruggenmerg, die zorgen voor
het bewegen van de skeletspieren. In de meeste
gevallen raakt een patiënt met ALS binnen enkele
jaren geheel verlamd. Uiteindelijk verliest hij (of
minder vaak zij) alle mogelijkheden tot bewegen,
eten en spreken, terwijl het bewustzijn wél volledig
intact blijft.
Rond 1930 kreeg de toen
beroemde basketballer Lou Gehrig amyotrofische
lateraalsclerose en dat maakte op het Amerikaanse
publiek zoveel indruk dat men de ziekte daar sinds
die tijd Lou Gehrig's ziekte is blijven noemen.
Gehrig ging na twee jaar dood aan longontsteking. In
uitzonderingsgevallen kan de ziekte milder verlopen.
Zo leeft de beroemde Britse astrofysicus Stephen
Hawking al dertig jaar met ALS, waarvan de helft in
een rolstoel.
Familiair bepaald
ALS is een zeldzame ziekte,
die bij ongeveer 1 op 100.000 mensen voorkomt. Bij
een klein gedeelte van de patiënten is de ziekte
familiair bepaald. Onlangs hebben onderzoekers uit
Amerika, Canada, België en Australië onder leiding
van Robert Brown van het Massachusetts General
Hospital in Boston bij 13 families met deze
erfelijke vorm van amyotrofische lateraalsclerose
kunnen aantonen dat de ziekte gekoppeld aan een
mutatie van het enzym superoxide-dismutase-1 (SOD-1)
op chromosoom 21 overerft (Nature, 4 maart
1993).
Superoxide-dismutase
beschermt het lichaam tegen de schadelijke werking
van vrije zuurstofradicalen. Die ontstaan bij
allerlei chemische reacties in ons lichaam. Elk
zuurstofatoom of -molecuul met in de buitenste
atoomschillen een ongepaard elektron is een vrije
radicaal. Door dat eenzame elektron heeft zo'n
molecuul een buitengewoon grote neiging om een
elektron weg te trekken van een ander molecuul. Dat
molecuul wordt dan weer een nieuwe radicaal. Zo kan
één radicaal een hele keten van reacties opwekken.
Zoiets leidt plaatselijk tot ernstige weefselschade.
Deze reactieve
zuurstofgroepen zijn weliswaar gevaarlijk, maar toch
onmisbaar. De afweercellen gebruiken ze bijvoorbeeld
om bacteriën te vernietigen. Als een afweercel door
een aangeboren defect geen vrije radicalen kan
aanmaken dan faalt het intracellulaire
dodingsmechanisme en blijven de bacteriën binnen in
de afweercel gewoon doorgroeien (chronische
granulomateuze ziekte). Radicalen worden
bijvoorbeeld ook in de lever gebruikt om giftige
stoffen af te breken.
Anti-oxidantia
Radicalen zijn dus
noodzakelijk voor de afweer. Radicalen ontstaan
bovendien onontkoombaar op plaatsen in het lichaam
waar zuurstof wordt verbruikt, en dat is vrijwel
overal waar energie wordt verbruikt. Om de schade
door kettingreacties van radicalen te verhinderen
gebruiken levende wezens een heel scala aan
anti-oxidantia die radicalen wegvangen. Daartoe
behoren vitamine C en vitamine E en verder een stof
als glutathion. Er zijn ook enzymen die als
anti-oxidans werken, zoals het bovengenoemde
superoxide-dismutase (SOD). SOD zorgt voor de
verwijdering van het superoxide-radicaal (O2 -.).
Op het eerste gezicht lijkt
de ontdekking van een mutatie in het
superoxide-dismutase bij amyotrofische
lateraalsclerose alleen van belang voor specialisten
(en misschien op den duur voor patiënten). ALS is
echter niet zo maar een zeldzame ziekte: het staat
in het middelpunt van de neurologische research,
omdat bij deze ziekte, net als bij de veel vaker
voorkomende dementie van Alzheimer of de ziekte van
Parkinson, bepaalde groepen zenuwcellen zonder
duidelijke oorzaak wegschrompelen en verdwijnen: er
zijn geen vaatafwijkingen, geen
ontstekingsverschijnselen en er is geen enkele
histologische verklaring te vinden.
Alle drie deze ziekten komen
vooral op latere leeftijd voor, tussen 50 en 70
jaar. In sommige gevallen zijn de ziekten duidelijk
familiair; ze kunnen zelfs tegelijk in één familie
voorkomen. De rol van vrije radicalen bij ALS is dus
van groot belang: men zou weleens dezelfde
verklaring kunnen vinden voor de andere veel minder
zeldzame degeneratieve ziekten van het zenuwstelsel.
Onlangs werd er in het
tijdschrift Proceedings of the National Academy
of Sciences of the USA (1993;90:178-82) nog een
andere genetische afwijking naar voren geschoven als
oorzaak voor ALS. Daarin werd aangetoond dat er ook
een mutatie in het gen GluR5 op chromosoom 21 is die
samen met ALS overerft. De mutatie in het eiwit
GluR5 zou afwijkende glutamaatreceptoren opleveren.
Zenuwcellen met een dergelijke receptor zouden
abnormaal heftig reageren op glutamaat. Glutamaat is
de belangrijkste stimulerende overdrachtsstof in het
centraal zenuwstelsel. Deze ontdekking past fraai
binnen de al langer bestaande theorie dat ALS het
resultaat is van langdurige overstimulatie van
zenuwcellen door glutamaat (excitotoxiciteit). Die
theorie is onder andere gebaseerd op de ontdekking
dat de consumptie van glutamaatachtige stoffen door
bewoners van het eiland Guam, in de vorm van de
pitten van de sagopalm, leidt tot een ALS-achtig
ziektebeeld. Bovendien zijn er bij sommige patiënten
met ALS abnormaal hoge concentraties glutamaat
aangetoond. Dat heeft toen geleid tot een hetze
tegen het voedingsadditief mono-natriumglutamaat,
dat als smaakversterker gebruikt wordt.
Het verband met de vrije
radicalen is dat glutamaat binnen de zenuwcel een
lichte stijging van het superoxide-radicaal
veroorzaakt. Een jarenlange inwerking van een
overmaat aan dit superoxide zou de excitotoxiciteit
veroorzaken. De ontdekking van een mutatie in het
superoxide-dismutase gen sluit daar dus mooi bij
aan. ALS zou dus meerdere oorzaken kunnen hebben:
het zou het resultaat kunnen zijn van een overmaat
aan glutamaat, een abnormaal overgevoelige
glutamaatreceptor of van een gestoorde functie van
SOD. In alle gevallen ontstaat er dan een overmaat
aan superoxide en dus excitotoxiciteit.
Cavia's
De ontdekkers van de mutatie
in het superoxide-dismutase gen opperen dat
patiënten met amyotrofische lateraalsclerose een
experimentele behandeling moeten krijgen met
anti-oxidantia. Het gekke is dat dit in het
Academisch Medisch Centrum in Amsterdam al sinds de
vijftiger jaren wordt gedaan. De vroegere professor
Hartog-Jager is daar al mee begonnen, toen hij
onderzoek deed naar de rol van het dieet bij ALS.
Hij toonde aan dat cavia's die voer zonder
anti-oxidanten kregen allemaal een ALS-achtig
ziektebeeld kregen.
In het AMC heeft men echter
onlangs laten zien dat het toedienen van
anti-oxidanten niet voldoende is om ALS te genezen.
Het hoofd van de neurologische kliniek, prof.
J.M.B.V. de Jong, heeft dan ook zijn twijfels bij de
uitspraak dat radicaalvangers ALS kunnen
verminderen: "In 1992 hebben we een dubbelblind
onderzoek afgesloten naar het effect van
anti-oxidanten bij 110 patiënten met ALS. De helft
van deze mensen kreeg een hoge dosis van de
anti-oxidans N-acetylcysteïne (NAC) en de andere
helft een placebo. We hebben maar een heel
bescheiden positief effect geboekt: de placebo-groep
overleed na een jaar en de NAC-groep na anderhalf
jaar. Bij geen enkele patiënt stabiliseerde het
ziektebeeld: ze gingen alleen iets minder snel
achteruit."
Het toedienen van een flinke
dosis vitamine C, E of een middel als NAC lijkt dus
geen afdoende therapie tegen een overmaat aan vrije
radicalen. Dergelijke behandelingen worden in de
alternatieve geneeskunde met graagte toegepast om
allerlei kwalen te behandelen. Megadoses vitaminen
worden wel geadviseerd tegen het verouderen van ons
lichaam. Het probleem met vrije radicalen is echter
dat deze heel plaatselijk ontstaan - bij ALS binnen
motorische zenuwcellen - en ter plekke reageren met
andere eiwitten. Een behandeling met een
anti-oxiderend geneesmiddel moet dus precies op de
juiste tijd, op de juiste plaats en in de juiste
dosering worden toegepast. Dat kon weleens de
achilleshiel van iedere behandeling met
anti-oxidanten blijken te zijn. Bron: Bartmeyer van
Putten
Universiteit Maastricht:
Trefwoorden:
Zuurstofradicalen,
Geneesmiddeltoxiciteit
en Superoxide Dismutase
Promotie drs.
G.J.M. den Hartog
in de Faculteit
der Geneeskunde
Titel: "Superoxide
dismutase as toxicity
modulator".
Promotores: Prof.dr.
A. Bast; Prof.dr. W.J.F.
van der Vijgh, VUA,
Co-promotor: dr. G.R.M.M.
Haenen.
Woensdag 18 juni 2003,
12.00 uur
Doxorubicine is een zeer
effectief antitumor
geneesmiddel. Een
ernstige bijwerking, die
de toepassing van dit
geneesmiddel hindert, is
de mogelijk fatale
hartschade.
Zuurstofradicalen lijken
een belangrijke rol te
spelen bij het ontstaan
van deze hartschade.
Antioxidanten zijn
stoffen die deze
zuurstofradicalen
onschadelijk kunnen
maken. Dit proefschrift
beschrijft onderzoek met
als voornaamste
conclusie dat het
antioxidant enzym
superoxide dismutase de
hartschade ten gevolge
van doxorubicine kan
voorkomen in muizen.
Gelukkig wordt de
antitumor werking van
doxorubicine niet
verminderd door
superoxide dismutase.
Dit biedt nieuwe
perspectieven om de
behandeling met
doxorubicine veiliger en
effectiever te maken |
|
|
Wikipedia:
Superoxide dismutase is een
essentieel enzym dat
zuurstofradicalen in organismen 'opruimt'. De reactie die
het enzym versnelt is voor zover bekend de allersnelste in de
biochemie. Superoxide dismutase is een klasse van enzymen,
welke een aantal verschillende metaalkernen kunnen hebben als
actief centrum. Dit kan ijzer, koper/zink, mangaan of nikkel
zijn. Het is afhankelijk van het gebruikte metaal welke
ligandomgeving er is. De koper/zink variant is het effectiefst
voor zover bekend. De koper/zink superoxide dismutase versnelt
de volgende reactie:
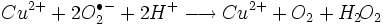
De overall-reactie bestaat in feite uit
de volgende twee reacties:

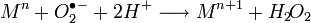
Opvallend hierbij is dat het enzym zowel
Cu (I) als Cu(II) laat reageren met superoxide, het
zuurstofradicaal. Hierdoor kan het enzym altijd actief zijn,
zowel met een eenwaardig als met een tweewaardig koperatoom
gebonden in het enzym. Hierdoor kan de reactie zo supersnel
plaatsvinden. H2O2 wordt vervolgens
"opgeruimd" door
katalase, een enzym dat grofweg een factor 1000 langzamer
werkt als superoxide dismutase.
Het is overigens ook niet voor niets dat
superoxide dismutase zo snel reageert. Superoxide behoort
namelijk tot de reactiefste moleculen, en zou praktisch met
alles reageren wat het aan moleculen tegenkomt, dus ook met
bijvoorbeeld DNA. Het snel opruimen van de radicalen is dan ook
noodzakelijk. De radicalen komen zo nu en dan vrij als "ongeluk"
bij diverse reacties.
Kooter IM
30 p in in English, 2004 |
| RIVM rapport 630111001
|
|
download pdf (241Kb) |
| |
|
|
Gamma-mangostin, a micronutrient of mangosteen fruit, induces
apoptosis in human colon cancer cells.
Source
Department of Pharmacognosy, School of Pharmacy, College of Pharmacy, and
Center of e-CAM, Taipei Medical University, 250 Wusing St., Taipei 110,
Taiwan.
Abstract
Recently colorectal
cancer rates have increased rapidly in Taiwan. The treatment of
colorectal cancer
includes surgery, radiation therapy and chemotherapy. Mangosteen (Garcinia
mangostana) is a famous Asian tropical fruit. γ-Mangostin is a
xanthone derivative
isolated from the fruit hull. In previous studies, we found evidence of
anti-inflammatory and anti-brain tumor activities in γ-mangostin. In this
study, we performed further studies to assess the apoptotic effects of
γ-mangostin on colorectal adenocarcinoma cells HT29. γ-Mangostin showed
concentration and time-dependent cytotoxic effects on HT29 cells.
Microscopic observation under Giemsa staining showed that γ-mangostin
induced cellular swelling and the appearance of apoptotic bodies,
characteristic of apoptosis in HT29 cells. In addition, flow cytometry
analysis showed an increase of hypodiploid cells in γ-mangostin-treated HT29
cells, while enhancement of intracellular peroxide production was detected
in the same γ-mangostin-treated cells by DCHDA assay and DiOC6(3) staining.
In view of the above results, γ-mangostin has demonstrated anticancer
activity and induces apoptosis in HT29 colorectal adenocarcinoma cells.
The evidence suggests that γ-mangostin
could serve as a micronutrient for colon
cancer
prevention and is a potential lead compound for the development of
anti-colon
cancer agents.
 |
 |

contact print
zoeken |
|
|
|
|
|
|
|
|
|
Metaalarbeider op
de gevoelige toer
Bron:
Nieuwsbrief Universiteit Leiden 5 juli 2005
|
Koperman
Biochemicus Armand Tepper
is, zoals hij zelf zegt, een
‘koperman’. Hij hoort bij de
onderzoeksgroep van prof. Gerard
Canters, waarin wordt gewerkt
aan metaaleiwitten. Dat zijn
eiwitten waaraan metaal-ionen
gebonden zijn. Het metaal maakt
dat het eiwit in een levende cel
een hele reeks van functies kan
uitvoeren, die voor eiwitten
zonder metaal meestal te hoog
gegrepen zijn. Haemoglobine in
het bloed is een bekend
voorbeeld van een
metaaleiwit, maar ook het
fotosynthetische systeem zit vol
met metalen. Ook bij het proces
dat energie uit suikers haalt
zijn veel metaaleiwitten
betrokken. |

Armand Tepper |
|
|
|
|
Helderblauw
Metaaleiwitten zijn niet alleen van
levens-belang in een organisme, maar
maken ook het leven van een
wetenschapper gemak-kelijker. Met
gebruik van metaaleiwitten kun je
namelijk een hele reeks spectroscopische
technieken toepassen die met gewone
eiwitten niet mogelijk zijn, zoals
speciale variaties op NMR. Een voordeel
is alleen al dat metaaleiwitten een
mooie kleur hebben, waardoor ze goed te
onderscheiden zijn. ‘Wij zien de mooiste
kleuren’, zegt Tepper. ‘Vooral koper en
ijzer zijn heel mooi. Hae-moglobine is
diep rood. En bepaalde koper-eiwitten
hebben een prachtige helderblauwe
kleur.‘ |

Metaaleiwitten hebben vaak een
kleur.
Links nitriet reductase en rechts
pseudoazurine, beide kopereiwitten |
|
|
Bionanotechnologie
Met die spectroscopische
technieken kunnen onderzoekers meer te
weten komen over de functie van het
metaal in het eiwit. Heel precies op
atomair niveau kunnen ze tegenwoordig de
mechanismen van eiwitten ontrafelen.
Tepper: ‘Eiwitten zijn grote en zeer
complexe moleculen. Maar we zijn nu
zover dat we een beetje begrijpen hoe
het werkt, en dat we die kennis ook
kunnen toepassen. Dan zit je op het
terrein van de bionanotechnologie.’
Elektronenverkeer
Een van de eigenschappen van
metaaleiwitten is dat ze
elektronenverkeer mogelijk maken als ze
reageren met andere stoffen: ze nemen
elektronen op of staan ze af. Dat
gebeurt tijdens de zogenoemde
redox-processen. ‘Redox’ is een
samentrekking van reductie en oxidatie.
Het molecuul dat een elektron afstaat
heet geoxideerd, en het molecuul dat er
een elektron bij krijgt heet
gereduceerd.
Biosensor
Tepper zelf gaat kopereiwitten
inzetten als hulpmiddel om een radicaal
nieuwe procedure te testen voor het
maken van een biosensor. Daarbij maakt
hij gebruik van die redox-processen. Een
biosensor is een sensor waarin
biologische elementen zijn geïntegreerd.
Biosensoren zijn handig, want
biologische moleculen zijn heel
specifiek. Tepper: ‘Neem de bekendste,
de glucosesensor, waarmee glucose
gemeten kan worden in het bloed. Die is
gebaseerd op een gespecialiseerd eiwit
dat in het lichaam glucose
metaboliseert. Zo’n eiwit heeft dus als
enige
target dat glucosemolecuul. Een
biosensor op basis van dat eiwit
is daarom een heel gerichte detector,
die allerlei ballast buiten beschouwing
laat.’ |
Elektrisch stroompje
Er is op het ogenblik veel
belangstelling voor metaaleiwitten als
component van een biosensor, juist
vanwege die elektronen-overdracht bij
chemische reacties. Die maakt namelijk
heel eenvoudige detectiemethoden
mogelijk, zegt Tepper.
‘Elektronenoverdracht betekent: een
elektrisch stroompje. En een elektrisch
stroompje kun je vrij gemakkelijk
meten.’ Om een biosensor te maken
immobiliseert Tepper een kopereiwit op
een vaste drager. Naar dat eiwit stuurt
hij elektronen toe met behulp van een
elektrode. Met die elektroneninjectie
lokt hij een chemische reactie uit van
het eiwit met het molecuul dat hij wil
detecteren. In zijn geval is dat
nitriet. |

Het principe achter een biosensor
gebaseerd op redoxeiwitten |
| |
|
Nitriet
Nitriet, bekend van voedselindustrie
en afvalwater, is een klein maar
belangrijk molecuul in levende cellen.
Het bestaat uit één stikstofatoom en
twee zuur-stofatomen. Nitriet wordt
spontaan gevormd bij de afbraak van NO,
stikstof-monoxide. De
nitrietconcentratie is dus een maat voor
de hoeveelheid afgebroken NO. En NO is
het molecuul waar het Tepper eigenlijk
om te doen is.
Mystery Molecule
Werd stikstofmonoxide (NO) vroeger
uitsluitend gezien als een giftig
uitlaatgas, sinds de tweede helft van de
jaren ‘80 is bekend dat dit gas een
signaalfunctie heeft bij heel veel
cruciale fysiologische processen. Het
reguleert bijvoorbeeld de bloeddruk, en
speelt daarom een belangrijke rol in het
onderzoek naar hart- en vaatziekten. Ook
geniet stikstofmonoxide nu bekendheid
als neurotransmitter en als stimulator
van het immuunsysteem. Al deze
ontdekkingen hebben geleid tot een ware
NO-hype in het onderzoek, culminerend in
een Nobelprijs in 1998. Het probleem met
deze ‘mystery molecule’ is dat
hij binnen tien seconden wordt
afgebroken in het bloed. Maar daarbij
komt dus het nitriet vrij dat Tepper
graag wil meten. Het gespecialiseerde
kopereiwit dat hij in zijn biosensor
gebruikt is nitriet reductase, dat in de
natuur betrokken is bij de omzetting van
nitriet.Isolator
Maar als dit het enige was zou
Tepper zijn Veni-subsidie helemaal niet
nodig hebben. Er is echter een probleem:
het metaalcentrum zit heel diep in het
eiwit opgeborgen. In de natuur heeft dat
een functie: de eiwitlaag wordt benut
ten behoeve van de specificiteit,
bijvoorbeeld voor de herkenning van een
ander eiwit. Of om alleen dát molecuul
aan het metaal te laten binden dat moet
worden omgezet. Elektronoverdracht is zo
alleen mogelijk door interactie met
specifieke partnermoleculen, terwijl
onbedoelde processen worden voorkomen.
Maar voor een wetenschapper is het
daardoor heel moeilijk om een stroom
elektronen te laten lopen van de
elektrode naar het metaal in het eiwit;
het eiwit werkt als een isolator. Dit
principiële probleem, zegt Tepper, heeft
een vertragende werking gehad op de
ontwikkeling van biosensoren die
gebaseerd zijn op redox-eiwitten. Wat
hij dus gaat doen is een radicaal nieuwe
methode testen om dat probleem aan te
pakken.
Patent
Hoe hij die eiwit-weerstand denkt te
gaan overwinnen kan hij op dit moment
nog niet zeggen, hoewel hij er alle
vertrouwen in heeft dat het gaat lukken.
Beter gezegd: juist omdat
hij daar alle vertrouwen in heeft.
Tepper denkt namelijk dat het idee
interessant zou kunnen zijn voor een
patent. En informatie voor een patent
geef je niet prijs.
Interdisciplinair
Na een onderzoeksperiode in Napels
is Tepper terug in de
metaaleiwittengroep van Gerard Canters,
bij wie hij in maart promoveerde op een
ander kopereiwit. In die groep voelt hij
zich thuis. Er zijn in Nederland niet
zoveel groepen die gespecialiseerd zijn
in metaaleiwitten. Het is daarbij een
heel goede groep, vindt hij. Juist op
het gebied van die kopereiwitten. Met
zijn onderzoek komt Tepper steeds meer
in interdisciplinair vaarwater terecht,
wat hij als pure winst beschouwt. Vooral
de bionanotechnologie ziet hij als zijn
tweede vaderland. ‘Al heel lang voel ik
de behoefte om meer toegepast onderzoek
te doen. Ik denk heel erg technisch, en
ik houd van het oplossen van
technologische problemen.’ |
|
|
3D
Ook in zijn vrije tijd is Armand
Tepper met scheikunde bezig, maar dan op
een artis-tieke manier. Hij heeft altijd
veel geschilderd, en raakte gaandeweg
geïnteresseerd in het maken van
driedimensionale beelden op de computer:
fotorealistische afbeeldingen van
moleculen. ‘Je kunt wetenschap zo
artistiek maken als je wilt’, vindt hij.
Het was gewoon een hobby, maar van het
een kwam het ander, en steeds vaker
weten belangstel-lenden hem te vinden.
Hij werkt nu samen met zijn vriending
die grafisch vormgever is.
Zie voor meer artistiek werk:
www.phantatomix.com/whatwedo.htm |

Artistieke impressie van het actieve
centrum van het enzym CuZn superoxide
dismutase |
|
|
|
| Bron: Bart Meijer van
Putten. |
.